Aktivitas Elektrokimia Bahan Elektroda Positif Baterai Ion Natrium P{{0}}Nax[Mg0.33Mn0.67]O2
Pengarang:ZHANG Xiaojun1, LI Jiale1,2, QIU Wujie2,3, YANG Miaosen1, LIU Jianjun2,3,4
1. Pusat Teknologi Sains Provinsi Jilin untuk Konversi Bersih dan Pemanfaatan Biomassa Bernilai Tinggi, Universitas Tenaga Listrik Timur Laut, Jilin 132012, Tiongkok
2. Laboratorium Utama Negara untuk Keramik Kinerja Tinggi dan Struktur Mikro Prima, Institut Keramik Shanghai, Akademi Ilmu Pengetahuan Tiongkok, Shanghai 200050, Tiongkok
3. Pusat Ilmu Material dan Teknik Optoelektronik, Universitas Akademi Ilmu Pengetahuan Tiongkok, Beijing 100049, Tiongkok
4. Sekolah Ilmu Kimia dan Material, Institut Studi Lanjutan Hangzhou, Universitas Akademi Ilmu Pengetahuan Tiongkok, Hangzhou 310024, Tiongkok
Abstrak
Dengan keunggulan biaya rendah dan distribusi bahan baku yang luas, baterai natrium-ion dianggap sebagai bahan alternatif terbaik untuk bahan katoda baterai lithium-ion. Pada fasa P2-NaMnO2 dengan struktur berlapis, larutan padat biner dari lapisan logam transisi dapat secara efektif meningkatkan kinerja elektrokimia bahan elektroda. Pada penelitian ini, model struktur larutan padat ion Mg Nax[Mg0.33Mn0.67]O2 dibangun dengan menggunakan model Coulomb. Perhitungan prinsip pertama menunjukkan bahwa tegangan pelepasan Nax[Mg{{10}}.33Mn0.67]O2 mencapai 3.0 V pada kandungan ion natrium lebih sedikit dari {{20}},67. Analisis kepadatan keadaan elektronik dan populasi muatan menunjukkan bahwa larutan padat Mg memotivasi aktivitas elektrokimia anionik oksigen kisi dalam fase P2-Nax[Mg0.33Mn0.67]O2, yang mengubah mekanisme reaksi elektrokimia dari sistem dari reaksi redoks sinergis kationik dan anionik menjadi reaksi redoks anionik reversibel. Transformasi ini memberikan metode baru untuk desain bahan elektroda untuk baterai ion Na, serta pendekatan baru untuk optimalisasi dan eksplorasi baterai ion lainnya.
Kata kunci:baterai ion natrium; aktivitas elektrokimia; prinsip pertama; doping logam alkali
TOB NEW ENERGY menyediakan set lengkapbahan baterai, mesin baterai, solusi lini produksi bateraidan teknologi baterai untuk baterai solid state, baterai ion natrium, dan pembuatan baterai lithium ion.
Dalam beberapa tahun terakhir, dengan adanya pemasaran industri energi baru seperti energi angin dan energi surya, masyarakat semakin menuntut teknologi penyimpanan energi skala besar[1,2]. Dalam penelitian bahan penyimpan energi, aktivitas elektrokimia dan stabilitas struktur bahan elektroda menjadi salah satu fokus penelitian [3,4]. Di antara berbagai sistem penyimpanan energi yang dikenal saat ini, bahan baterai lithium-ion relatif matang dan banyak digunakan. Namun, masalah seperti distribusi sumber daya litium yang tidak merata dan sulitnya teknologi pemulihan litium telah membatasi penerapan baterai litium-ion dalam skala besar[5, 6, 7]. Natrium yang satu keluarga dengan litium memiliki ciri bahan baku melimpah, harga murah, dan distribusi luas. Pada saat yang sama, baterai natrium-ion memiliki sifat fisik dan kimia serta mekanisme reaksi elektrokimia yang mirip dengan baterai lithium-ion. Oleh karena itu, baterai natrium-ion adalah salah satu bahan alternatif yang paling menjanjikan [8,9].
Berthelot dkk.[10]menemukan bahwa dalam oksida berlapis NaTMO2 yang mengandung logam transisi tunggal (TM), ion natrium dan kekosongan diatur dalam lapisan natrium murni, menghasilkan banyak platform tegangan untuk jenis oksida ini selama proses pelepasan. . Hal ini mengakibatkan penurunan cepat kapasitas spesifik dan penurunan kinerja siklus secara signifikan, sehingga efisiensi konversi energi oksida jenis ini rendah. Unsur-unsur larutan padat dimasukkan ke dalam lapisan logam transisi untuk membentuk susunan campuran logam transisi biner atau bahkan multi-elemen. Bahan elektroda mengandung sejumlah besar muatan yang tidak teratur, yang secara efektif dapat menekan platform tegangan di atas dan meningkatkan efisiensi konversi energi. Yabuuchi et al.[11]menggunakan Na2CO3, (MgCO3)4Mg(OH)2·5H2O dan MnCO3 sebagai bahan baku. Reaksi keadaan padat dilakukan pada suhu 900 derajat selama 12 jam untuk memperoleh bahan elektroda Na2/3[Mg1/3Mn2/3]O2 fasa P2 biner yang tidak teratur dengan larutan padat Mg. Mereka menemukan bahwa pada rapat arus 10 mA/g, kapasitas spesifik awal bahan katoda fase P2 Na2/3[Mg1/3Mn2/3]O2 yang disiapkan adalah sekitar 150 mAh/g[11]. Sedikit lebih rendah dari kapasitas spesifik Na2/3MnO2 (184 mAh/g). Bruce dkk.[12]menemukan bahwa meskipun terdapat reaksi elektrokimia oksigen kisi dalam fase P2 Na2/3[Mg1/3Mn2/3]O2, tidak ada pengendapan oksigen yang teramati. Hal ini menunjukkan bahwa pengenalan Mg meningkatkan reversibilitas siklus dan kapasitas spesifik material yang dapat dibalik. Namun, selama proses pengisian dan pengosongan, mekanisme reaksi elektrokimia mikroskopis dari kisi oksigen dalam sistem ini masih belum jelas, dan mekanisme dimana larutan padat Mg meningkatkan stabilitas sistem juga masih belum jelas.
Oleh karena itu, penelitian ini mengambil fasa P2 Nax[Mg0.33Mn0.67]O2 sebagai objek penelitian dan mengadopsi metode penghitungan prinsip pertama teori fungsional densitas (DFT). Sebuah studi sistematis tentang aktivitas elektrokimia dan stabilitas struktural kinerja pelepasan bahan katoda Nax[Mg0.33Mn0.67]O2 dengan larutan padat ion Mg telah dilakukan. Untuk memperjelas mekanisme mikroskopis bahan elektroda dalam reaksi elektrokimia pada skala mikro elektron dan atom, maka akan memberikan acuan pemahaman proses elektrokimia dan perancangan bahan baru.
1 Metode perhitungan
Perhitungan dalam karya ini didasarkan pada paket VASP perangkat lunak berbasis gelombang bidang [13,14] teori fungsional kerapatan. Metode gelombang bidang aditif digunakan [15], dan fungsi korelasi pertukarannya adalah pendekatan gradien umum (GGA) dalam bentuk Perdew-Burker-Ernzerhof [13,16]. Parameter Hubbard U diperkenalkan untuk mengoreksi elektron d Mn, dan nilai U efektif adalah 3,9 eV[17,18]. Energi pemutusan gelombang bidang bawah adalah 600 eV. Ketika relaksasi ion selesai, gaya pada semua atom menjadi kurang dari 0.1 eV·nm-1. Saat mengoptimalkan struktur kristal, digunakan struktur supercell 3×3×1 (72 atom), konstanta kisi adalah 0.874 nm×0.874 nm×1.056 nm, dan k- titik grid zona Brillouin adalah 3×3× 3[19]. Metode fonon beku digunakan untuk menghitung spektrum getaran kisi dalam paket perangkat lunak Phonopy. Untuk menghindari pengaruh kondisi batas periodik, struktur supercell 3×3×1 digunakan untuk menghitung konstanta gaya dan spektrum fonon fase P2 NaMnO2 dan Na[Mg0.33Mn0.67]O2. Model muatan titik Coulomb digunakan untuk menghitung pendudukan ion struktur desodium dengan cepat, dan konfigurasi pendudukan Na dengan energi Coulomb terendah dipilih untuk perhitungan prinsip pertama yang lebih akurat [20]. Tegangan pelepasan bahan elektroda dapat dinyatakan sebagai [20]:
$V=-\frac{G(\text{N}{{\text{a}}_{{{x}_{2}}}}\text{M }{{\text{O}}_{2}})-G(\text{N}{{\text{a}}_{{{x}_ {1}}}}\text{M}{{\text{O}}_{2}})-({{x}_{2}}-{{x}{ {16}}{1}})G(\text{Na})}{({{x}_{2}}-{{x}_{1}}){{ e}^{-}}}$
Dimana G adalah energi total sistem yang bersesuaian, dan e- adalah muatan elemen[21].
2 Hasil dan diskusi
2.1 Karakteristik mikrostruktur dan stabilitas struktur
The space group of the P2 phase NaMnO2 structure is R$\bar{3}m (Fig. 1)[22,23]. The spatial configuration of the Mg solid solution Na0.67[Mg0.33Mn0.67]O2 structure is similar to that of NaMnO2. Mg ions replace 1/3 of the Mn ions in the transition metal layer. The theoretical ion ratio of Mg to Mn is 1:2. Experimental characterization found that at this ratio, Mg ions in the Nax[Mg0.33Mn0.67]O2 structure only form disordered arrangements with Mn, retaining the order of the Na layer[24]. When the ion ratio Mg:Mn>1:2, Mg, Na, dan Mn akan membentuk susunan kation yang tidak teratur. Seperti yang ditunjukkan pada Gambar 1(A), mode penumpukan oksigen kisi adalah ABBA..., Mg dan Mn masing-masing menempati situs oktahedral di antara lapisan oksigen AB, dan Na menempati situs prisma segitiga antara lapisan oksigen AA dan BB[ 25,26]. Seperti yang ditunjukkan pada Gambar 1(B), terdapat susunan sarang lebah Mg dan Mn pada lapisan logam transisi[27], yang mirip dengan susunan antara Li dan Mn dalam senyawa kaya litium[28]. Oktahedron [MgO6] disusun dengan 6 oktahedron [MnO6] yang berbagi tepi[29,30]. Pada lapisan logam alkali struktur Na0.67[Mg0.33Mn0.67]O2, terdapat dua situs kisi untuk ion natrium. Yang satu disusun dengan lapisan atas dan bawah dari oktahedron [MgO6] atau [MnO6] yang berbagi tepi. Yang lainnya disusun secara sebidang dengan lapisan atas dan bawah oktahedron [MgO6] atau [MnO6].
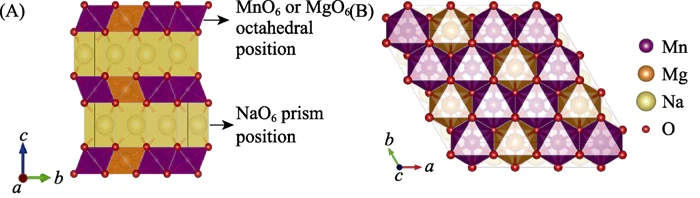
Gambar 1 Diagram skema P2-Na2/3[Mg1/3Mn2/3]O2
Dalam struktur dengan kandungan ion natrium berbeda, ion natrium dipengaruhi oleh interaksi Coulomb antara Mn dan Mg pada lapisan logam transisi dan ion Na pada lapisan logam alkali, menunjukkan dua mode pendudukan yang berbeda. Oleh karena itu, pekerjaan ini pertama-tama menggunakan model Coulomb untuk menyaring dengan cepat konfigurasi fase P2 Na0.67[Mg0.33Mn0.67]O2 dengan energi Coulomb terendah. Untuk memverifikasi rasionalitasnya, kami menghitung dan mensimulasikan pola XRD dari konfigurasi yang disaring ini dan membandingkannya dengan hasil yang diukur [11]. Hasilnya ditunjukkan pada Gambar 2. Perhitungan (016) dan (110) sedikit bergeser ke kanan dibandingkan dengan karakterisasi eksperimental, yang terutama disebabkan oleh adanya struktur amorf dan cacat di beberapa bidang kristal bahan yang disiapkan secara eksperimental. . Struktur model komputasi merupakan struktur kristal sempurna, sehingga terdapat deviasi tertentu antara pelebaran XRD dan intensitas puncak simulasi komputasi dengan hasil eksperimen. Selain itu, terdapat susunan ion Na pada dua bidang kristal ini, dan penyisipan serta pelepasan ion Na merupakan kemungkinan alasan lain terjadinya pergeseran posisi puncak yang sesuai. Setelah mempertimbangkan efek di atas, bentuk puncak dan intensitas XRD yang disimulasikan konsisten dengan hasil eksperimen, dan model yang dibangun dapat mereproduksi informasi mikrostruktur dalam eksperimen, yang menunjukkan bahwa struktur yang disaring secara teoritis relatif akurat dan dapat diandalkan[31,32 ].

Gambar 2 Perbandingan pola XRD terhitung dan eksperimental Na0.67[Mg0.33Mn0.67]O2
Untuk mempelajari pengaruh larutan padat Mg terhadap stabilitas struktur, kami menggunakan prinsip pertama yang dikombinasikan dengan "metode fonon beku" untuk menghitung spektrum getaran kisi P{{0}}NaMnO2 dan P{{2} }Na[Mg0.33Mn{{10}}.67]O2. Seperti yang ditunjukkan pada Gambar 3, gelombang pemilik tidak memiliki frekuensi imajiner di seluruh zona Brillouin, yang menunjukkan bahwa P2-Na[Mg0.33Mn0.67]O2 memiliki stabilitas dinamis. Dengan membandingkan spektrum fonon kedua material, ditemukan bahwa doping Mg tidak mengubah rentang frekuensi getaran secara signifikan dan berdampak kecil pada getaran kisi. Struktur yang didoping Mg juga menunjukkan stabilitas dinamis yang baik. Selain itu, Bruce dkk. berhasil menyiapkan fase P2 Na[Mg0.33Mn0.67]O2 dengan larutan padat Mg, yang selanjutnya menunjukkan bahwa material tersebut memiliki stabilitas termodinamika tambahan. Oleh karena itu, tidak sulit untuk melihat bahwa P2-Na[Mg0.33Mn0.67]O2 memiliki stabilitas struktural yang baik.

Gambar 3 Kurva dispersi fonon (A) NaMnO2 dan (B) Na0.67[Mg0.33Mn0.67]O2
2.2 Analisis sifat elektrokimia fasa P2 Nax[Mg1/3Mn2/3]O2
Untuk mempelajari pengaruh doping Mg terhadap sifat elektrokimia bahan, kami menghitung tegangan pelepasan struktur larutan padat Mg P{{0}}Nax[Mg0.33Mn{{7} }.67]O2 (Gambar 4). Kisaran konsentrasi ion Na ditentukan secara eksperimental, yaitu 0.11 Kurang dari atau sama dengan x Kurang dari atau sama dengan 0.66[11].Gambar 4(A) menunjukkan struktur berubah selama proses pelepasan, dan voltase yang sesuai (Gambar 4(B)) terutama mencakup tiga platform: 3,4, 2,9, dan 2,1 V. Kapasitas teoretis yang diprediksi adalah 152 mAh/g, yang pada dasarnya konsisten dengan hasil eksperimen[11] . Kurva tegangan pelepasan yang dihitung dari prinsip pertama sedikit lebih tinggi dari hasil pengukuran sebenarnya. Alasan utamanya adalah perhitungan prinsip pertama mengabaikan pengaruh kondisi pengukuran eksperimental, seperti elektrolit, konduktivitas ion litium, suhu pengukuran eksperimental, dll. Penelitian kami sebelumnya menunjukkan [33] bahwa meskipun kurva tegangan pelepasan yang dihitung lebih tinggi daripada yang diukur secara eksperimental kurva, tren perubahan secara keseluruhan konsisten. Oleh karena itu, dapat dianggap bahwa selama seluruh proses pelepasan, tegangan Nax[Mg0.33Mn0.67]O2 konsisten dengan hasil eksperimen[12,20]. Kapan x<66%, Nax[Mg0.33Mn0.67]O2 has a high voltage of about 3.0 V, and there is no obvious additional voltage platform, indicating that the substitution of Mg2+ for Mn3+ has the effect of inhibiting sodium ion rearrangement and structural phase change. Previous charge and discharge studies on NaMnO2 and other systems have found that the orderly arrangement of transition metals is usually accompanied by more voltage platforms.

Gambar 4 (A) perubahan struktural yang dihitung DFT dan (B) kurva tegangan pelepasan P2-Nax[Mg0.33Mn0.67]O2 selama pelepasan
Dalam keadaan ideal, keadaan valensi Mg dan Mn dalam Na2/3[Mg0.33Mn0.67]O2 berturut-turut adalah +2 dan +4, dan tidak dapat dilanjutkan untuk dioksidasi ke keadaan valensi yang lebih tinggi. Oleh karena itu, tidak ada aktivitas elektrokimia kation dalam sistem, dan proses pengisian dan pengosongan material merupakan reaksi elektrokimia anion. Dalam Na0.67MnO2, keadaan valensi awal ion Mn adalah +3.33. Selama proses pengisian, ion Mn dapat mentransfer elektron 0,67 ke luar hingga mencapai valensi stabil +4. Pada saat ini, semua Na+ telah dilepaskan, dan oksigen kisi tidak pernah berpartisipasi dalam reaksi elektrokimia[34]. Oleh karena itu, proses pengisian dan pengosongan Na0.67MnO2 muncul sebagai reaksi elektrokimia kationik. Banyak penelitian menunjukkan bahwa ketika jumlah elektron yang hilang oleh oksigen kisi kurang dari 0.33, reaksi elektrokimia anionik memiliki reversibilitas yang baik[11-12,28]. Oksidasi anion oksigen yang berlebihan (jumlah elektron yang hilang lebih besar dari 0.33) menyebabkan konfigurasi elektron oksigen menyimpang dari aturan stabil delapan penggandeng, mengakibatkan reaksi transformasi ireversibel dan pembentukan ikatan OO. Hal ini bahkan dapat menyebabkan evolusi oksigen dan pengisian serta pelepasan struktur elektroda yang tidak dapat diubah [27,35]. Dalam Na0.67[Mg0.33Mn0.67]O2, jika keadaan batas kehilangan muatan dipertimbangkan. Artinya, ketika ion Na terlepas sepenuhnya membentuk struktur Na0[Mg{{40}}.33Mn0.67]O2, Mg dan Mn selalu mempertahankan {{ 45}} dan +4 valensi. Anion O dioksidasi menjadi valensi -1,67, kehilangan elektron 0,33, yang lebih rendah dari batas reaksi elektrokimia anion ireversibel. Oleh karena itu, dalam keseluruhan reaksi pengisian Na0.67[Mg0.33Mn0.67]O2, oksigen kisi tidak perlu ditata ulang secara spasial, dan reaksi elektrokimia bersifat reversibel. Pengenalan Mg2+ tidak hanya mempertahankan kapasitas spesifik yang dapat dibalik, tetapi juga meningkatkan kepadatan energi material dengan meningkatkan tegangan pelepasan.
Untuk membuktikan aktivitas elektrokimia oksigen dalam bahan Nax[Mg{{0}}.33Mn0.67]O2 selama proses pelepasan, kami menghitung kepadatan keadaan elektronik (Gambar 5) untuk keadaan awal dan struktur pelepasan akhir material. Ditemukan bahwa selama proses pelepasan, ion Na secara bertahap tertanam, jumlah elektron dalam sistem meningkat, dan tingkat Fermi berpindah ke tingkat energi yang lebih tinggi. Jumlah lubang pada orbit O2p berangsur-angsur berkurang, menunjukkan bahwa elektron yang memasuki sistem dipindahkan ke orbit kosong oksigen kisi, dan oksigen kisi berkurang. Selama proses pelepasan bahan elektroda, oksigen kisi berpartisipasi dalam reaksi elektrokimia anion. Pada saat ini, hampir tidak ada perubahan pada elektron orbital Mn-d, dan tidak ada perpindahan muatan, yaitu keadaan valensi Mn tidak berubah selama proses pelepasan, membuktikan bahwa Mn tidak aktif secara elektrokimia[12, 36]. Namun, selama proses pelepasan P2-NaxMnO2, elektron terus mengisi orbital kosong Mn dan O berenergi tinggi, yang menunjukkan bahwa Mn dan O aktif secara elektrokimia dan merupakan reaksi elektrokimia tipikal di mana anion dan kation bekerja sama .

Gambar 5 Kerapatan elektron keadaan (A) P2-Nax[Mg0.33Mn0.67]O2 dan (B) P2-NaxMnO2 pada Na yang berbeda kandungan ion selama pelepasan
PDOS: proyeksi kepadatan negara bagian
Kesimpulan yang konsisten dapat ditarik melalui analisis populasi biaya (Gambar 6). Selama proses pelepasan Nax[Mg0.33Mn0.67]O2, jumlah muatan ion Mn pada dasarnya tidak berubah, sehingga tidak ikut serta dalam reaksi elektrokimia; pada proses peningkatan kandungan Na dari 0.11 menjadi 0.66 diperoleh ion O sekitar 0.2e- . Terjadi pengisian muatan yang signifikan, menunjukkan aktivitas elektrokimia anionik [37]. Melalui analisis populasi muatan P2-NaxMnO2, ditemukan bahwa seiring dengan meningkatnya kandungan Na, Mn dan O bersama-sama berpartisipasi dalam reaksi elektrokimia. Hasil ini konsisten dengan analisis keadaan kerapatan elektronik. Terbukti bahwa larutan padat Mg mengubah mekanisme reaksi elektrokimia sistem dari reaksi elektrokimia kooperatif anion dan kation menjadi reaksi elektrokimia anion yang dapat dibalik, dan proses ini tidak mempengaruhi reversibilitas pengisian dan pengosongan material.

Gambar 6 Analisis muatan (A) Nax[Mg0.33Mn0.67]O2 dan (B) P2-NaxMnO2 pada kandungan ion natrium yang berbeda
3 Kesimpulan
Penelitian ini menggunakan perhitungan prinsip pertama untuk mempelajari secara sistematis karakteristik mikrostruktur, stabilitas kinetik dan aktivitas elektrokimia larutan padat Mg2+ fase P2 Nax[Mg1/3Mn2/3]O2. Pengenalan Mg2+ mengubah jenis reaksi elektrokimia bahan dari reaksi elektrokimia kooperatif anionik dan kationik NaxMnO2 menjadi reaksi elektrokimia anionik reversibel Nax[Mg{{10}}.33Mn{ {16}}.67]O2. Ketika anion O dalam P2-Nax[Mg0.33Mn0.67]O2 berpartisipasi dalam reaksi elektrokimia, rentang perolehan dan kehilangan muatan kurang dari 0,33, yang berarti baik reversibilitas. Pengenalan Mg2+ tidak hanya meningkatkan tegangan pelepasan material, tetapi juga mempertahankan kapasitas spesifik material yang dapat dibalik, dan pada akhirnya meningkatkan kepadatan energi material.
Pada material elektroda ion natrium, memasukkan logam alkali tanah ke dalam lapisan logam transisi untuk larutan padat kationik adalah strategi pengoptimalan kinerja material baru. Mekanisme dasarnya adalah memicu aktivitas elektrokimia anion dengan mengorbankan aktivitas elektrokimia kation, mengubah mekanisme reaksi elektrokimia material, meningkatkan tegangan pelepasan, dan pada akhirnya mengoptimalkan kepadatan energi material. Strategi ini tidak hanya memberikan metode baru dalam perancangan bahan elektroda untuk baterai natrium-ion, namun juga memberikan ide-ide baru untuk optimalisasi dan eksplorasi baterai ion lainnya.
Referensi
[1] HU YING-YING, WEN ZHAO-YIN, RUI-KUN, dkk. Status penelitian dan pengembangan baterai natrium yang canggih. Sains dan Teknologi Penyimpanan Energi, 2013,2(2):81-90.
[2] SHEN GUAN-YE, LI CHEN, XU BING-LIANG, dkk. Alokasi ekonomi untuk sistem penyimpanan energi dengan mempertimbangkan tenaga angin. Jurnal Universitas Tenaga Listrik Timur Laut, 2018,38(4):27-34.
[3] MA CHAO, ZHAO XIAO-LIN, KANG LI-TAO, dkk. Bahan anoda dikarboksilat tak terkonjugasi untuk sel elektrokimia. Angew. kimia. Int. Edisi, 2018,57(29):8865-8870.
[4] RICHARDS WD, DACEK ST, KITCHAEV DA, dkk. Fluorinasi bahan katoda oksida logam transisi berlebih litium. Bahan Energi Tingkat Lanjut, 2018,8(5):1701533.
[5] XIANG XING-DE, ZHANG KAI, CHEN JUN. Kemajuan terkini dan prospek bahan katoda untuk baterai natrium-ion. Adv. Mater., 2015,27(36):5343-5364.
[6] MA CHAO, ZHAO XIAO-LIN, HARRIS MM, dkk. Asam urat sebagai senyawa aktif secara elektrokimia untuk baterai ion natrium: mekanisme penyimpanan Na+- bertahap dari konjugasi π dan anion karbon yang stabil. Materi & Antarmuka Terapan ACS, 2017,9(39):33934-33940.
[7] LEE DH, XU JING, MENG Y S. Katoda canggih untuk baterai Na-ion dengan kecepatan tinggi dan stabilitas struktural yang sangat baik. Fis. kimia. kimia. Fis., 2013,15(9):3304-3312.
[8] KUBOTA K, YABUUCHI N, YOSHIDA H, dkk. Oksida berlapis sebagai bahan elektroda positif untuk baterai Na-ion. Buletin MRS, 2014,39(5):416-422.
[9] CLÉMENT RJ, BRUCE PG, GREY CP. Tinjauan—oksida logam transisi tipe P2-berbasis mangan sebagai bahan katoda baterai ion-natrium. Jurnal Masyarakat Elektrokimia, 2015,162(14):A2589-A2604.
[10] BERTHELOT R, CARLIER D, DELMAS C. Investigasi elektrokimia diagram fase P2-NaxCoO2. Nat. Mater., 2011,10(1):74-80.
[11] YABUUCHI N, HARA R, KUBOTA K, dkk. Bahan elektroda baru untuk baterai natrium yang dapat diisi ulang: P2-tipe Na2/3[Mg0.28Mn0.72]O2 dengan kapasitas reversibel yang sangat tinggi. J.Materi. kimia. J, 2014,2(40):16851-16855.
[12] MAITRA U, HOUSE RA, SOMERVILLE JW, dkk. Kimia redoks oksigen tanpa kelebihan ion logam alkali dalam Na2/3[Mg0.28Mn0.72]O2. Nat. Kimia, 2018,10(3):288-295.
[13] GUO SHAO-HUA, SUN YANG, YI JIN, dkk. Memahami difusi ion natrium dalam oksida P2 dan P3 berlapis melalui eksperimen dan perhitungan prinsip pertama: jembatan antara struktur kristal dan kinerja elektrokimia. Materi NPG Asia, 2016,8:e266.
[14] JI HUI-WEI, KITCHAEV DA, LUN ZHANG-YAN, dkk. Investigasi komputasi dan realisasi eksperimental katoda Li-ion berkapasitas tinggi yang tidak teratur berdasarkan redoks Ni. Kimia Bahan, 2019,31(7):2431-2442.
[15] LEE J, URBAN A, LI XIN, dkk. Membuka potensi oksida gangguan kation untuk baterai litium yang dapat diisi ulang. Sains, 2014,343(6170):519-522.
[16] URBAN A, LEE J, CEDER G. Ruang konfigurasi oksida tipe rockalt untuk elektroda baterai litium berkapasitas tinggi. Bahan Energi Tingkat Lanjut, 2014,4(13):1400478.
[17] CHAKRABORTY A, DIXIT M, AURBACH D, dkk. Memprediksi sifat katoda yang akurat dari bahan oksida berlapis menggunakan fungsi kepadatan meta-GGA SCAN. Bahan Komputasi npj, 2018,4:60.
[18] PERKOTAAN A, ABDELLAHI A, DACEK S, dkk. Asal usul struktur elektronik dari gangguan kation pada oksida logam transisi. Fis. Pendeta Lett., 2017,119(17):176402.
[19] ASSAT G, TARASCON J M. Pemahaman mendasar dan tantangan praktis aktivitas redoks anionik dalam baterai Li-ion. Energi Alam, 2018,3(5):373-386.
[20] YABUUCHI N, NAKAYAMA M, TAKEUCHI M, dkk. Asal usul stabilisasi dan destabilisasi dalam reaksi redoks solid-state ion oksida untuk baterai lithium-ion. Nat. Kommun., 2016,7:13814.
[21] SANNYAL A, AHN Y, JANG J. Studi prinsip pertama pada siligene dua dimensi (2D SiGe) sebagai bahan anoda baterai ion logam alkali. Ilmu Material Komputasi, 2019,165:121-128.
[22] LI HONG, HU YONG-SHENG, PAN HUI-LIN, dkk. Kemajuan penelitian struktur material elektroda baterai penyimpan ion natrium suhu kamar. Scientia Sinica Chimica, 2014,44(8):1269-1279.
[23] WANG YUE-SHENG, XIAO RUI-JUAN, HU YONG-SHENG, dkk. Elektroda dengan gangguan kation P2-Na0.6[Cr0.6Ti0.4]O2 untuk baterai natrium-ion simetris berkecepatan tinggi yang dapat diisi ulang. Nat. Kommun., 2015,6:6954.
[24] WANG QIN-CHAO, MENG JING-KE, YUE XIN-YANG, dkk. Menyetel material katoda terstruktur P2-dengan substitusi Mg situs Na untuk baterai Na-ion. Selai. kimia. Sosial, 2019,141(2):840-848.
[25] MENDIBOURD A, DELMAS C, HAGENMULLER C. Interkalasi elektrokimia dan deinterkalasi perunggu NaxMnO2. Pers Akademik, 1985,57(3):323-331.
[26] SOMERVILLE JW, SOBKOWIAK A, TAPIA-RUIZ N, dkk. Sifat fase "Z" pada katoda baterai Na-ion berlapis. Ilmu Energi & Lingkungan, 2019,12(7):2223-2232.
[27] QU JIE, WANG DONG, YANG ZU-GUANG, dkk. Penyesuaian katoda komposit yang diinduksi oleh doping-situs-variasi: studi kasus terowongan lapisan Na0.6MnO2 dengan doping Mg2+ di lokasi Na/Mn. Aplikasi ACS. Materi. Antarmuka, 2019,11(30):26938-26945.
[28] SATO T, SATO K, ZHAO WEN-WEN, dkk. Oksida tipe garam batu dengan gangguan kation yang metastabil dan berukuran nano: meninjau kembali stoikiometri LiMnO2 dan NaMnO2. Jurnal Kimia Material A, 2018,6(28):13943-13951.
[29] GUIGNARD M, DELMAS C. Menggunakan baterai untuk mensintesis vanadium oksida baru. Pilihan Kimia, 2017,2(20):5800-5804.
[30] WANG PENG-FEI, YAO HU-RONG, LIU XIN-YU, , dkk. Gangguan Na+/ kekosongan menjanjikan baterai Na-ion berkecepatan tinggi. Kemajuan Sains, 2018, 4(3): eaar6018.
[31] KIM H, KIM DJ, SEO DH, dkk. Studi ab initio tentang interkalasi natrium dan fase perantara dalam Na0.44MnO2 untuk baterai natrium-ion. Kimia Bahan, 2012,24(6):1205-1211.
[32] LI XIN, MA XIAO-HUA, SU DONG, dkk. Visualisasi langsung efek Jahn-Teller digabungkan dengan pengurutan Na dalam Na5/8MnO2. Nat. Mater., 2014,13(6):586-592.
[33] WANG YOUWEI, WANG JUNKAI, ZHAO XIAOLIN, dkk. Mengurangi potensi kelebihan muatan baterai Li-O2 melalui desain katoda penyelarasan pita. Ilmu Energi & Lingkungan, 2020,13(8):2540-2548.
[34] ZHENG C, RADHAKRISHNAN B, CHU IH, dkk. Pengaruh pencampuran logam transisi pada pemesanan Na dan kinetika lapisan oksida P2. Tinjauan Fisik Diterapkan, 2017,7(6):064003.
[35] LUN ZHENG-YAN, OUYANG B, CAI ZI-JIAN, dkk. Prinsip desain untuk katoda garam batu gangguan kation berbasis Mn berkapasitas tinggi. Kimia, 2020,6(1):153-168.
[36] SEO DH, LEE J, URBAN A, dkk. Asal struktural dan kimia dari aktivitas redoks oksigen dalam bahan katoda kelebihan Li yang berlapis dan tidak tertata kation. Nat. Kimia, 2016,8(7):692-697.
[37] BAI QIANG, YANG LU-FENG, CHEN HAI-LONG, dkk. Studi komputasi bahan elektroda dalam baterai natrium-ion. Bahan Energi Tingkat Lanjut, 2018,8(17):1702998.





